에슬리카바제핀 아세테이트의 효과와 안정성: 단일기관의 경험
Efficacy and Safety of Eslicarbazepine Acetate: A Single-Center Experience
Article information
Trans Abstract
Background
Eslicarbazepine acetate (ESL) is a third-generation anti-seizure drug used in patients with focal-onset seizures. This retrospective study aimed to evaluate the efficacy and safety of ESL for the treatment of epilepsy in a real-world clinical setting.
Methods
From March 2022 to April 2023, the medical records of patients with epilepsy who were prescribed ESL at Gyeongsang National University Changwon Hospital were analyzed. Efficacy outcomes were assessed based on seizure frequency, while safety outcomes included the occurrence of adverse events.
Results
In total, 93 patients were included in the analysis. Over the 1-year follow-up period, ESL demonstrated a significant reduction in seizure frequency. Seventy patients (75.3%) achieved seizure freedom (including 19 patients who were seizure-free for more than 1 year before taking ESL) and 78 patients (86.7%) experienced seizure reduction. Adverse events were reported in 16 patients (17.2%), with the most commonly observed being hyponatremia (5.4%), dizziness (4.3%), seizure aggravation (3.2%), and somnolence (2.2%).
Conclusions
In this real-world setting, ESL demonstrated sustained efficacy in reducing seizure frequency over 1 year of treatment. The overall safety profile was acceptable. Hyponatremia occurred at a higher frequency than previously known but improved after the discontinuation or reduction of the drug. These findings support the use of ESL as an effective and well-tolerated option for long-term epilepsy treatment in real-world clinical practice.
서론
에슬리카바제핀 아세테이트(eslicarbazepine acetate, ESL)는 하루 한 번 경구로 복용하는 항경련제로 전압의존성 소디움 채널(voltage-gated sodium channel, VGSC)에 작용해서 VGSC의 느린 비활성화(slow inactivation)를 통해 발작을 억제한다. 3개의 무작위 배정 임상시험(randomized controlled trials, RCT)의 결과를 토대로1-3 유럽에서는 2009년에 국소발작(focal-onset seizure) 치료에 부가요법(adjunctive therapy)으로 사용을 승인받았고, 미국에서는 2013년에 승인받았다. 이후에 단독요법(monotherapy)에 대한 2개의 RCT를 바탕으로4,5 단독요법으로 사용도 승인받았다. 우리나라는 이보다 늦은 2020년 11월에 식품의약품안전처의 승인을 받아 국소발작의 치료에 사용되기 시작하였다. 외국에는 ESL이 10년 이상 사용되면서 실제 임상에서의 효과와 부작용에 대한 여러 연구가 발표되었으나 우리나라에는 도입된 기간이 짧아 이러한 자료가 부족한 실정이다. 이에 본 연구는 외래에서 1년간 ESL을 사용한 경험을 바탕으로 효과와 안정성에 대해 살펴보고자 한다.
방법
2022년 3월부터 2023년 4월 사이에 창원경상국립대학교병원 신경과를 방문한 뇌전증 환자 중에서 ESL을 처방받은 환자 106명의 의무기록을 후향적으로 검토하였다. 이들 중 ESL을 처방받은 이후 외래를 방문하지 않아 유효성과 안정성을 평가할 수 없는 13명은 제외하고 93명의 임상 데이터를 분석하였다.
본 기관에서는 뇌전증 환자의 진료 시에 발작 발생 여부와 이상반응 유무를 확인하고 의무기록에 기록한다. 유효성 평가를 위해서 대상자들이 ESL을 복용하기 전 1년 동안 발작의 빈도를 확인하였고, ESL을 복용한 이후 발작의 빈도 변화를 의무기록 검토를 통해 확인하였다. 안정성 평가를 위해서 ESL 복용 후 발생한 이상반응도 조사하였다. 본 연구는 창원경상국립대학교병원 임상시험 심사위원회의 승인 및 환자 동의 면제 승인을 받아 진행하였다(No. 2023-07-023).
결과
1. 대상자 정보
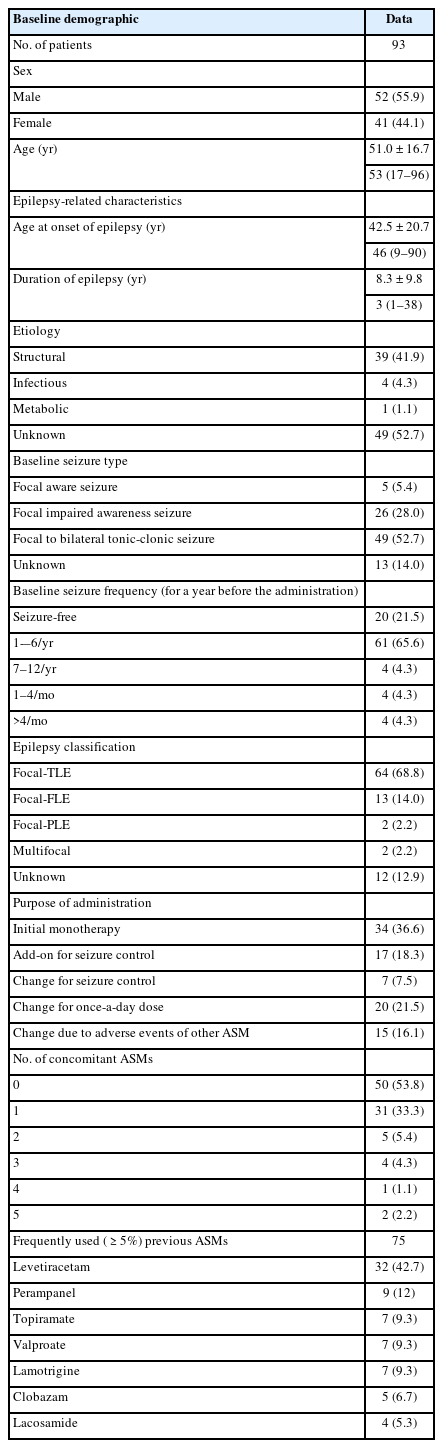
연구에 포함된 93명 중 여자가 41명(44.1%)이었고, 93명의 평균 나이는 51세였다. 뇌전증을 진단받은 나이는 평균 42.6세였고, 뇌전증의 평균 유병기간은 6.9년이었다. 뇌전증 유형에 따라 분류하면, 측두엽뇌전증이 64명 (68.8%)으로 가장 많았고, 다음으로 전두엽뇌전증 13명(14.0%), 미분류(undetermined) 12명(12.9%) 순이었다. 발작 유형에 따른 분류에서는 양측 강직간대발작으로 이행하는 국소발작(focal to bilateral tonic-clonic seizure)이 49명(52.7%), 인식장애를 동반한 국소발작(focal impaired awareness seizure)이 26명(28.0%), 미분류 13명(14.0%) 순이었다. 뇌전증의 원인에 따른 분류에서는 원인미상(unknown)이 49명(52.7%), 구조적 이상 39명(41.9%), 감염 4명(4.3%) 순이었다. ESL을 투여한 목적은 뇌전증 최초 진단 후 단독요법으로 복용한 경우가 34명(36.6%)으로 가장 많았고, 하루 한 번 복용하는 편의성을 위해서 변경한 경우가 20명(21.5%), 발작 조절을 위해 부가요법으로 복용한 경우가 17명(18.3%)이었다. ESL을 부가요법으로 복용한 경우 levetiracetam을 함께 복용하고 있는 경우가 가장 많았다(Table 1). 전체 93명 중 20명은 ESL 복용 직전 1년 동안 발작이 없었는데, 이 중 13명은 하루 한 번 복용하는 편의성 때문에 ESL로 변경하였고, 나머지 7명은 기존에 사용하던 항경련제의 부작용으로 인해 ESL로 교체하였다.
2. 유효성
전제 93명의 대상자 중 ESL을 복용한 뒤 61명(65.6%)에서는 추적관찰 기간동안 발작이 발생하지 않았다. ESL 복용 직전 1년 동안 발작이 없었던 20명을 제외한 73명 중에서 59명(80.8%)은 발작 빈도가 감소하였고, 51명(69.9%)은 무발작(seizure freedom) 상태에 도달하였다(Fig. 1). 73명 중 부가요법으로 ESL을 사용한 대상자는 32명이었다. 이들 중 22명(68.8%)에서 발작 빈도가 감소하였고, 15명(46.9%)은 무발작 상태에 도달하였다(Fig. 2.). ESL을 단독요법으로 사용한 41명 중37명(90.2%)에서 발작 빈도가 감소하였고, 36명(87.8%)은 무발작에 도달하였다(Fig. 3.).
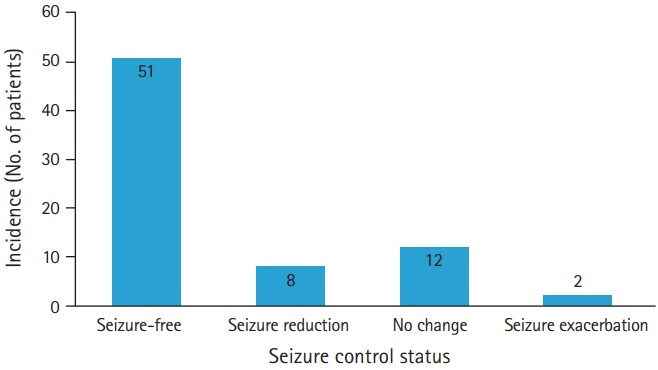
Seizure control status of all patients except those who were seizure-free. Of the 73 patients, 59 (80.8%) had reduced seizure frequency, and 51 (69.9%) reached seizure-free status. There was no change in seizure frequency in 12 patients, and seizures worsened in two patients.
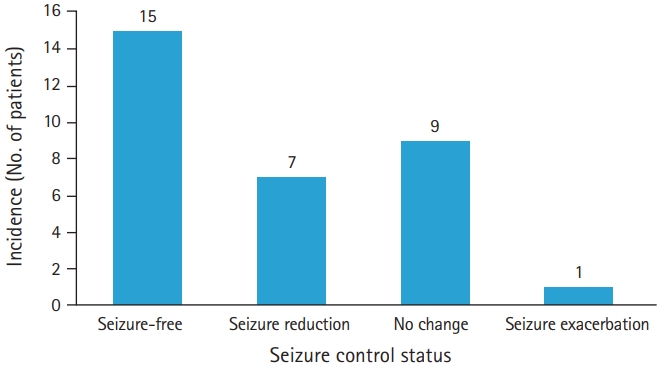
Seizure control status of the patients who received adjunctive therapy. Seizure frequency was reduced in 22 of 32 patients (68.8%) who took eslicarbazepine acetate as an adjunctive therapy, and seizure-free status was achieved in 15 (46.9%). Nine had no change in the frequency of seizures, and one had worsened seizures.
3. 안정성
93명의 대상자 중에서 16명(17.2%)에서 부작용이 발생하는데, 부작용의 종류와 부작용이 발생하였을 당시 ESL 용량은 Table 2에 기술하였다. 부작용은 저나트륨혈증이 5명(5.4%)으로 가장 많았고, 그 다음으로 어지럼 4명(4.3%), 발작 악화 3명(3.2%), 졸림이 2명(2.2%)에서 발생하였다(Fig. 4). ESL 부작용으로 약을 중단한 대상자는 7명(7.5%)이었다. 저나트륨혈증 2명(2.2%), 발작 악화 2명(2.2%), 그 외 어지럼, 발진, 구역으로 약을 중단한 경우가 각각 1명씩(1.1%)이었다. 저나트륨혈증이 발생한 5명의 평균 혈청 나트륨은 125.8 mEq/L (범위, 119.6–132.0 mEq/L)였다. 저나트륨혈증이 가장 심했던 1명만 어지럼을 호소하였고, 나머지 4명은 무증상이었다. 저나트륨혈증이 심했던 2명은 ESL 복용을 중단하였고, 다른 2명은 ESL 감량 후 호전되었다. ESL 복용 후 발작의 빈도가 증가한 대상자가 3명 있었다. 이들은 각각 뇌전증 초기 진단 후 단독요법으로 복용하거나 하루 한 번 복용하는 편의성이나 발작 조절을 위해서 항경련제를 교체한 경우였다.

Incidence of adverse events after taking eslicarbazepine acetate. Adverse events occurred in 16 patients (17.2%). There were five cases of hyponatremia (5.4%), four cases of dizziness (4.3%), three cases of seizure aggravation (3.2%), and two cases of somnolence (2.2%). Rash, nausea, blurred vision, restless, and dyspnea occurred in one patient (1.1%) each.
4. Oxcarbazepine에서 eslicarbazepine acetate로 변경
93명의 대상자 중 20명은 oxcarbazepine (OXC)를 복용하다가 동일 용량의 ESL로 교체하였다. 9명은 발작 조절을 위해서 교체하였고, 나머지 11명은 하루 한 번 복용하는 편의성 때문에 교체하였다. 11명은 OXC를 복용하면서 직전 1년 동안 발작이 없었는데 이 중 10명은 그대로 무발작 상태가 지속되었고 1명은 발작이 악화되었다. OXC를 복용하면서 무발작 상태가 아니었던 9명 중 4명은 ESL로 변경 후 무발작 상태가 되었고, 1명은 발작 횟수의 감소를 보였고, 3명은 변화가 없었으며, 나머지 1명은 발작이 악화되었다.
고찰
ESL은 3세대 항경련제로 carbamazepine (CBZ), OXC과 함께 dibenzazepine 계열의 약물로 공통된 화학구조(dibenzazepine neucleus)로 인해 많은 특징을 공유하지만 고리의 10, 11 자리에 케토 기(keto group)가 아닌 하이드록시 기(hydroxy group)가 결합함으로써 CBZ, OXC와 차이를 보인다. ESL은 CBZ과는 달리 대사산물로 부작용을 일으킬 수 있는 CBZ-10, 11-epoxide를 생성하지 않으므로 안정성 측면에서 유리하다. 또한 OXC은 체내에서 4:1의 비율로 (S)-licarbazepine과 (R)-licarbazepine으로 분해되는 반면 ESL은 20:1의 비율로 분해되어 주로 (S)-licarbazepine이 만들어진다.6-8 (S)-licarbazepine은 (R)-licarbazepine보다 혈액-뇌장벽을 잘 통과하고 더 효과적이며 부작용이 적으므로 ESL이 OXC보다 다 효과적으로 발작을 조절할 수 있을 것으로 생각된다.
국소발작 치료에 ESL을 사용한 14개의 임상연구를 종합한 결과가 2017년에 발표되었다. 2,058명의 환자 중 75.6%에서 발작이 절반 이하로 감소하였고, 41.3%는 무발작에 도달하였다.9 본 연구에서는 ESL 복용 직전 1년 동안 발작이 없었던 20명을 제외한 73명 중 80.8%에서 발작 빈도가 감소하였고, 69.9%가 무발작에 도달하였다. 선행연구에 비해서 본 연구에서는 무발작에 도달한 비율이 다소 높게 나타났다. 선행연구에서 전체 대상자의 발작 빈도의 중앙값이 월 3회였던 것에 비해, 본 연구에서는 ESL 복용 시작 전 1년 동안 발작이 6회 미만으로 비교적 빈번하지 않았던 대상자가 많이(61명) 포함되었던 점이 영향을 주었을 것이다. 또한 ESL 복용을 시작한 뒤 추적관찰 기간이 90일 미만으로 발작의 조절상태를 평가하기에 기간이 충분하지 않았던 대상자가 16명 포함되었던 점도 영향을 주었을 것으로 생각한다.
ESL을 국소발작 치료의 부가요법으로 사용하고 1년간 발작 조절 상태를 평가한 2개의 연구가 있다. 첫 번째 연구에는 239명의 대상자가 포함되었는데, 53.2%가 1년 뒤 발작이 절반 이하로 감소하였고 12.5%가 무발작에 도달하였다.10 다른 연구에서는 223명의 대상자 중 42.5%에서 발작이 절반 이하로 감소하였고, 10.8%에서 무발작 상태가 되었다.11 본 연구에서는 ESL을 부가요법으로 사용한 대상자는 32명이었고, 이 중 68.8%에서 발작 빈도가 감소하였으며, 46.9%은 무발작에 도달하였다. ESL을 부가요법으로 사용한 경우에서도 선행연구에 비해 무발작에 도달한 비율이 높았다. 선행연구에서 대상자의 발작 빈도의 중앙값이 월 7–9회로 비교적 발작이 잦았던 것에 비해,1,2 본 연구에 포함된 대상자들은 직전 1년 동안 발작의 빈도가 6회 미만이었던 대상자가 23명이나 포함되어 좋은 결과를 초래하였을 것으로 생각한다.
2017년에 발표된 14개의 임상연구를 종합한 결과에서 ESL 복용 후 34.0% (691/2,031)에서 부작용이 발생하였고, 어지럼(6.7%), 피로(5.4%), 졸음(5.1%), 저나트륨혈증(3.5%), 불안정/실조(3.4%)의 순으로 자주 발생하였다. 부작용으로 인해 ESL 복용을 중단한 대상자는 13.6% (267/1,960)였다. ESL 복용 중단을 초래한 부작용은 어지럼(2.3%), 피로(2.0%), 발진(1.5%), 졸음(1.5%) 순으로 나타났다.9 본 연구에서도 발생한 부작용의 종류는 선행연구와 유사했지만 저나트륨혈증이 5명으로 가장 높은 빈도(5.4%)로 발생하였다는 점이 달랐다. 저나트륨혈증은 CBZ나 OXC에서도 공통적으로 발생하는 부작용으로, 명확한 발생 기전은 밝혀지지 않았다. ESL로 치료받는 환자들의 0.6%–1.3%에서 발생하고 ESL의 용량이 증가함에 따라 나트륨의 농도가 더 낮아지는 경향이 있다. 또한 신장질환을 가지고 있거나 이뇨제나 CBZ와 같은 약물과 함께 복용할 때 저나트륨혈증이 더 자주 발생하는 것으로 알려져 있다.12 본 연구에서 저나트륨혈증이 발생한 5명이 복용하던 ESL의 농도는 800 mg이 4명, 1,200 mg이 1명이었고, ESL 복용량과 혈청 나트륨 농도 사이에 상관관계는 없었다. 5명 모두 동반한 신장질환은 없었고, 함께 복용하는 약 중에 저나트륨혈증을 발생시킬 수 있는 약은 없었다. 다만 일부 연구에서는 저나트륨혈증의 발생 빈도를 4.8%–6.6%로 비교적 높게 보고한 경우도 있어13 ESL 복용으로 발생하는 저나트륨혈증 빈도에 대해서는 향후 추가적인 연구가 필요해 보인다.
Elger 등14은 건강한 대상자에게 같은 용량의 ESL과 OXC를 복용하게 하고 eslicarbazepine과 (R)-licarbazepine의 혈중농도를 측정하였다. ESL을 복용한 군에서 발작 조절과 관련 있는 eslicarbazepine의 혈중농도는 높았고, 부작용과 관련 있는 (R)-licarbazepine은 낮았다. 뇌전증 환자를 대상으로 한 임상연구에서도 비슷한 결과가 확인되었다. 뇌전증 치료를 목적으로 OXC를 복용하다 효과 부족으로 ESL로 변경한 90명 중 56.5%는 발작 빈도가 절반 이하로 감소하였고, 23.5%는 무발작 상태가 되었다. 또한 부작용 때문에 ESL로 변경한 61명 중 39.5%에서만 다시 부작용이 발생하였다.15 이 결과를 볼 때 OXC를 ESL로 변경하면 발작 조절 효과는 높이고, 부작용은 줄이며, 하루 한 번 복용하는 장점으로 순응도를 높이는 것을 기대할 수 있다. 본 연구에서 20명이 OXC에서 동일 용량의 ESL로 교체하였는데, 9명은 발작 조절을 위해서, 나머지 11명은 하루 한 번 복용하는 편의성 때문에 교체하였다. 발작 조절을 위해서 ESL로 변경한 9명 중 4명은 무발작 상태가 되었고, 1명은 발작 횟수의 감소를 보였다. 이를 바탕으로 OXC를 복용하면서 발작이 충분히 조절되지 않거나 부작용이 발생한 경우 ESL로 변경을 고려해 볼 수 있다. 다만 본 연구에서 2명은 OXC에서로 변경한 뒤 오히려 발작이 악화되어 이에 대한 주의가 필요하다.
본 연구는 몇 가지 제한점을 가진다. 첫째, 전체 대상자 93명 중 ESL을 복용하기 직전 1년 동안 발작이 없었던 20명과 1년 동안 6번 미만의 비교적 적은 빈도의 발작을 경험하였던 61명이 포함되어 발작의 감소를 평가하는 데 제한이 있었다. 추적관찰 기간이 90일 미만으로 짧았던 17명이 포함되어 이 역시 발작 빈도의 변화를 평가하는 데 어려움을 더했다. 둘째, 대상자가 93명으로 많지 않았고, 의무기록 검토를 통해 시행된 후향적 연구 방법으로 인해 정확한 발작빈도 변화와 부작용 발생을 평가하는데 어려움이 있었다. 향후 잘 디자인된 전향적 다기관 연구를 통한 추가적인 검증이 필요하리라 생각한다.
Notes
Conflicts of interest
No potential conflicts of interest relevant to this article was reported.
Funding
None.
Author contributions
Conceptualization, Formal analysis: YTW. Data curation: KDH. Investigation, Visualization: KYS. Methodology, Project administration: KOY. Writing–Original Draft: Yang TW, Kim DH. Writing–Review & Editing: All authors.
All authors read and approved the final manuscript.