에슬리카바제핀 아세테이트: 약동력학과 약물 상호작용
Eslicarbazepine: Pharmacokinetics and Drug Interactions
Article information
Trans Abstract
Eslicarbazepine acetate is an advanced antiseizure medication that is an improvement upon carbamazepine and oxcarbazepine. This novel antiseizure medication regulates voltage-gated sodium channels and provides fewer adverse effects and better tolerability. Herein, we present the characteristics, pharmacokinetics, and drug interactions of eslicarbazepine acetate based on the research that has been conducted to date.
서론
Eslicarbazepine acetate (ESL)은 포르투갈의 Bial 사에서 개발한 항경련제로서, 1999년에 처음 소개되어 2009년에 유럽에서 사용 승인되었다.1 2013년에 미국 식품의약국(U.S. Food and Drug Administration)의 승인을 받았다. 우리나라에서는 2020년 말에 도입되어 사용되고 있는 약물로서, 유럽의 여러 나라에 비하여 약 10년 정도 늦게 도입된 셈이다.
ESL에 대해서 알아보기 위해서는 약물의 화학적 특징, carbamazepine이나 oxcarbazepine과의 관계 등을 이해할 필요가 있다. 이 종설에서는 ESL의 대한민국 도입에 맞춰서 약물의 특성과 약동학, 그리고 다른 약물과의 상호작용에 대해서 여러 연구에서 확인한 사실을 바탕으로 하나씩 짚어보겠다.
본론
1. 거울상이성질체(enantiomer)
화학에서 이성질체(isomer)란 동일한 분자식을 가진 서로 다른 구조의 분자를 말한다. 이성질체는 구조이성질체와 입체이성질체로 나뉜다. 구조이성질체는 분자식이 같지만 원자가 결합할 때 서로 다른 배열 또는 구조를 가진 것, 즉 분자식이 같지만 원자의 연결 구조가 다른 것이다. 입체이성질체는 구조적으로 같지만 공간에서 배열이 다른 화합물로서, 비대칭 중심(chiral center)이 있는 원자를 가지는 분자는 입체이성질체를 가질 수 있다. 이 때 서로 겹쳐지지 않는 분자 구조를 가진 입체이성질체를 거울상이성질체(enantiomer)라고 한다. 이러한 관계의 두 분자를 사람의 왼손과 오른손에 빗대어 카이랄(chiral)이라는 단어를 사용하는데, 이것은 ‘손’을 뜻하는 그리스어 ‘chiros’에서 유래되었다. 카이랄 분자를 명명하는 방법 중 R/S 명명법은 유기화합물에서 거울상이성질체를 나타내기 위해서 사용한다. 비대칭 중심의 치환기를 칸-인골드-프렐로그 순위 규칙에 따라 우선 순위를 붙이는데, 비대칭 중심을 회전시켜서 우선 순위가 가장 낮은 치환기를 관찰자에서 먼 방향에 두었을 때 나머지 치환기가 오른쪽으로 순위가 감소하는지 왼쪽으로 순위가 감소하는지에 따라서 분류한다. 오른쪽(시계 방향)으로 감소하면 R, 왼쪽(반시계 방향)으로 감소하면 S를 붙인다.2,3
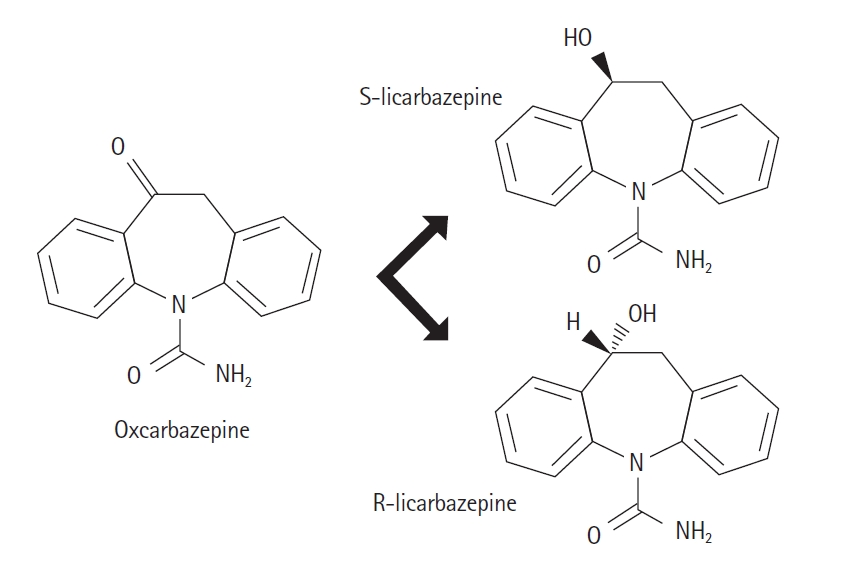
ESL은 carbamazepine과 oxcarbazepine의 5-카복사미드 치환기(carboxamide substitute)를 갖는 디벤자제핀핵(dibenzazepine nucleus)을 공유하지만 -10,11 위치에서 구조적인 차이가 있다. 이러한 분자 구조의 차이는 약물 대사의 차이를 만드는데, 바로 carbamazepine의 대사에서 독성을 가질 수 있는 carbamazepine-10,11-epoxide를 생성하지 않는 것이다. Oxcarbazepine는 carbamazepine-10,11-epoxide의 생성을 줄이는 목적으로 개량된 약물이며, 10-ketoreduction을 거쳐 10-hydroxy-carbazepine으로 대사된 후 licarbazepine이 되는 방식을 따른다.4 이 과정에서 oxcarbazepine은 S-licarbazepine과 R-licarbazepine이라는 두 개의 거울상이성질체로 대사된다. Oxcarbazepine가 대사되어 생성되는 S-licarbazepine과 R-licarbazepine의 비율은 4:1로 알려져 있다.5-7 그 결과 carbamazepine에 비하여 부작용의 빈도나 강도는 개선되었으나, 여전히 같은 종류의 부작용을 보이고 있다.6
ESL의 화학 구조는 (S)-10-acetoxy-10,11-dihydro-5H-dibenz[b,f]azepine-5-carboxamide로서(Fig. 1), 이전의 연구에 의하면 같은 분자량의 oxcarbazepine을 투여했을 때보다 S-licarbazepine에의 노출은 약 16%까지 증가한다.6,8,9 ESL이 대사되어 생성되는 S-licarbazepine과 R-licarbazepine의 비율은 약 20:1로 알려져 있다.
2. 전압의존성 소디움 통로(voltage-gated sodium channel)
ESL은 전압의존성 소디움 통로(voltage-gated sodium channel, VGSC)에 선택적으로 작용하는 약물이다. VGSC의 느린 비활성화(slow inactivation)을 주된 기전으로 하며, 지속적 Na+ 전류 (INaP)의 모순적 상향조절(upregulation)이 없다. 잘 알려져 있듯이, 신경의 흥분은 주로 Na+에 의해 결정된다. 활동 전위 곡선의 빠른 상승(음전위)은 신경세포의 Na+ 채널의 개방으로 인한 급격한 일시적 Na+ 내향 전류(INaT)에 의해 발생한다. 그러나 Na+ 채널의 일부는 탈분극이 진행되는 동안에도 개방된 상태로 남아있다. 이 INaP는 역치 이하의 전압 범위에서 활성화되며, 따라서 세포막 흥분성을 조절하는 데 중요한 역할을 하는 것으로 알려져 있다.
Carbamazepine은 VGSC의 과분극을 일으키는데, 역치 이하의 전압에서 INaP의 완연한 증가가 관찰되며 활성도나 전압에 따른 INaT의 비활성화가 이루어지지 않는다.10 이러한 현상을 INaP의 모순적 상향조절이라고 하며, 반복적인 신경 활성을 감소시키는 효과의 상실을 초래할 수 있다. 이것은 carbamazepine과 같이 Na+에 작용하는 약물에서 뇌전증에 대한 불응성을 설명하는 주요 기전 중의 하나로 알려져 있다. 반면 ESL은 INaP에 영향을 주지 않아 반복적인 신경 활성에 대해 억제 효과가 유지되는 것이 확인되어, carbamazepine에 대한 약물불응성을 극복할 수 있을 것으로 기대한다.11
한편, ESL은 carbamazepine과 oxcarbazepine에 비하여 빠르게 활성화되는 Nav1.3 소디움 통로에 대해서 carbamazepine에 비하여 비활성화된 소디움 통로에 대해 선택성이 더 높다.12 Nav1.7과 Nav1.8 소디움 통로에 대해서는 R-licarbazepine에 비하여 ESL이 약 5–10배의 친화성을 보여주었다.
3. 약물동력학
ESL은 eslicarbazepine의 전구약물로서(monohydroxy derivative), 구강으로 투여 후 빠르게 흡수되어 간에서 환원된다. S-licarbazepine의 생체이용률은 약 94%이다.13 S-licarbazepine은 cytochromes P450 (CYP) system에서 다시 oxcarbazepine과 R-licarbazepine으로 전환되기도 하지만, 그 양은 미미하다(Fig. 2).14 투여 후 first pass metabolism (또는 presystemic metabolism), 즉 전신 순환이 일어나기 전에 먼저 일어나는 대사에서 eslicarbazepine으로 전환되므로, oxcarbazepine 또는 R-licarbazepine이 생성되는 비율이 5% 내외가 된다.4,7,9 또한 ESL은 carbamazepine10,11-epoxide로 대사되지 않고 혈액 내 oxcarbazepine 및 R-licarbazepine을 낮게 유지하게 되는 oxcarbazepine에 비하여 약물동력학적으로 이득이 있다.
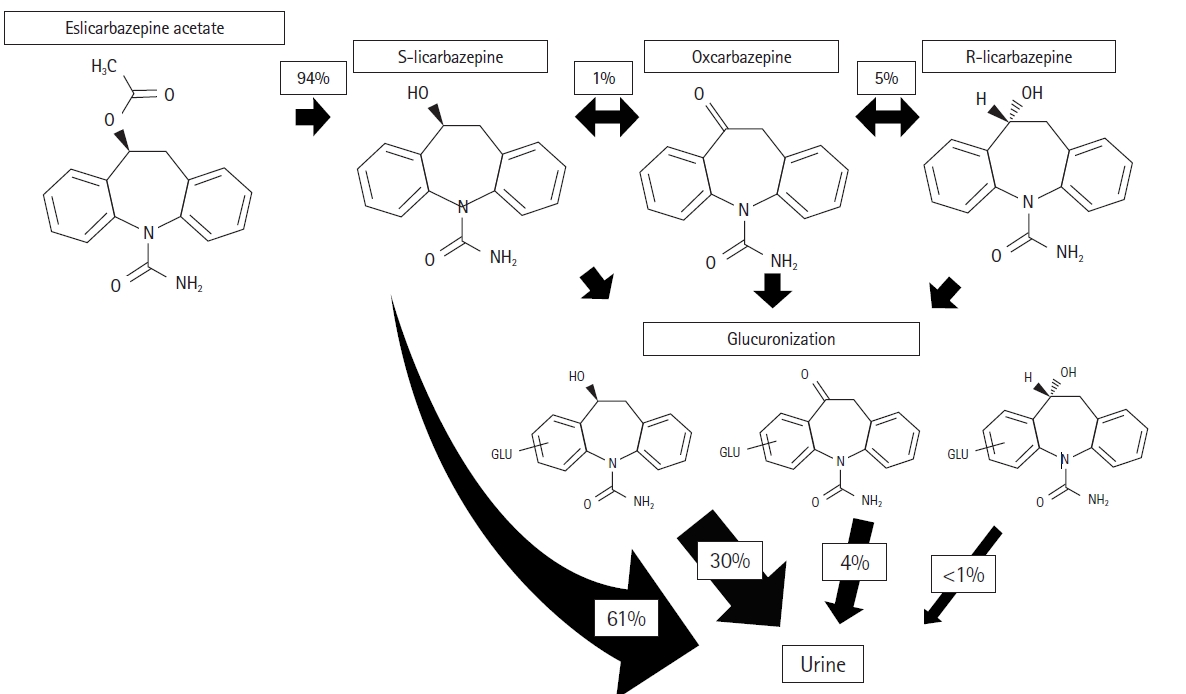
Metabolic pathways of eslicarbazepine acetate. Eslicarbazepine is eliminated in unchanged (60%) or glucoronated form (30%). The ratio of S-licarbazepine to R-licarbazepine is 20:1.
GLU, glucuronide.
ESL은 식사에 상관 없이 투여할 수 있으며,15 하루 두 번 투여한 경우보다 하루 한 번 투여한 경우에 혈중 최고 농도가 약 32% 높았고, 24시간 동안의 약물에의 노출을 곡선하면적(area under curve)로 나타냈을 때 하루 한 번과 하루 두 번의 용법에서 유의한 차이가 없었다.16 따라서 ELS은 하루 한 번 투여하는 것이 타당하다. ESL의 혈중 농도는 투여하는 약물의 용량과 관련이 있다. ESL 800 mg을 투여하는 경우 혈중 최저 농도와 최고 농도의 중간값은 각각 4.2 µg/mL와 15.5g/mL이며, 1,200 mg에서는 각각 8.9 µg/mL와 23.0 µg/mL로 보고되었다.6,17 건강한 성인을 대상으로 한 연구에서, ELS의 반감기는 단일 투여 후 약 9시간(ELS 20 mg)에서 17시간(ESL 1,200 mg)이었고 다회 투여 후에는 20시간에서 24시간이었다. ESL 400, 800, 1,200 mg을 반복적으로 구강으로 투여한 후 혈중 최고 농도에 도달하는 것은 약 2.5시간에서 3시간이었다.16 단백 결합은 약 30%이며,6 하루 한 번 투약으로 약 4, 5일 후에 혈액 내 농도가 안정상태에 이른다. ESL은 주로 소변으로 배출되는데, 약 2/3는 비결합 상태(free form)로 배출된다.16 투여되는 약물의 약 92%는 ESL으로 배출되며, 나머지는 R-licarbazepine, oxcarbazepine, ESL-glucuronide, R-licarbazepine-glucuronide, oxcarbazepine-glucuronide 등이다(Fig. 2). ESL의 약동학은 콩팥 기능에 영향을 받으므로,7,18 크레아티닌 청소율(creatinine clearance, Ccr)이 60 mL/min 이하인 경우 ESL의 용량을 절반으로 줄여서 사용해야 한다. 만약 Ccr이 <30 mL/min인 경우에는 ESL의 용량 결정에 대한 충분한 근거가 없다. 간 기능 이상이 있는 환자에서는 대조군과 비교하여 ESL의 혈중 농도의 통계적인 차이가 없었으며,19 특히 간문맥-체순환 단락(portal systemic shunt)가 있는 환자에서도 혈중 농도에서 유의한 차이가 없었다.
4. 약물 상호작용
ESL은 CYP2C9를 억제하는 것으로 알려져 있으며,20 CYP2C19에 대해서는 carbamazepine이나 oxcarbazepine의 활성물질인 licarbazepine에 의한 CYP2C19 억제와 유사하다.21 그 외의 CYP 동형 단백질(isoform)에 거의 영향이 없다. ESL은 clobazam, clonazepam, gabapentin, phenobarbital, phenytoin, lamotrigine, primidone, valproate에 의한 대사억제가 없다.
Carbamazepine과 함께 투여할 경우, ESL의 농도는 약 30%의 감소가 발생하지만 carbamazepine의 농도는 유의미한 차이가 없다.17,22 Phenytoin과 함께 투여할 경우 ESL의 농도는 약 33% 감소하며, phenytoin은 약 35% 증가한다.22,23 Phenobarbital에 의하여 ESL의 농도는 약 34% 감소한다.22 Valproic acid와 levetiracetam은 ESL를 투여해도 혈중 농도의 변화가 없으며,16,22 lamotrigine과 topiramate는 각각 약 14%와 18% 정도 감소한다.16,22,24 그러나 ESL은 valproic acid, levetiracetam, lamotrigine, 그리고 topiramate의 영향을 받지 않는다. Clobazam과 gabapentin은 ELS과 의미있는 상호작용이 알려지지 않았다. Carbamazepine, phenytoin, 그리고 phenobarbital은 용량 조절이 필요하지만, 그 이외의 항경련제와 병용할 경우에는 용량 조절의 필요성이 떨어진다.
ESL 1,200 mg/day와 병용투여할 경우에 ethinylestradiol/levonorgestrel로 구성된 경구피임약은 약 40% 내외의 감소가 발생하며, 이에 따라 800 mg 이상의 ESL을 복용할 경우에는 경구피임약의 용량 감소에 의한 피임 실패가 예상되므로 피임 방법의 변경을 고려해야 한다. 잘 알려진 바와 같이 oxcarbazepine에 의한 CYP3A 관련 대사 항진으로 경구피임약의 혈중 농도 감소가 발생하는데,25 ESL에 의한 경구피임약의 혈중 농도 감소도 같은 기전에 의한 것으로 알려져 있다.
Warfarin을 ESL 1,200 mg/day와 병용투여할 경우, S-warfarin에서 약 23%의 혈중 농도 감소가 확인되었으며, R-warfarin에서는 의미 있는 혈중 농도 감소가 없었다.26 그러나 실제 임상에서는 ESL과 warfarin을 병용투여하는 거의 모든 경우에 프로트롬빈 시간(prothrombin time) 국제표준화비율(international normalized ratio)의 추적 관찰이 필요하겠다. ESL은 혈중 지질 농도에 영향을 주지 않는 것으로 보고된 바 있으나,27 병용투여하는 rosuvastatin과 simvastatin의 혈중 최고 농도는 각각 61%–64%와 41%–60% 정도로 감소하는 것이 확인되었다.28,29 Atorvastatin과 ESL의 병용투여에 대한 연구는 이루어지지 않았으나, CYP450과 연관된 statin의 특성을 고려한다면 혈중 농도의 감소가 예상된다.27 Metformin과 digoxin은 ESL 1,200 mg/day의 병용투여에 영향을 받지 않는 것으로 보고되었다.7,30,31
정리
ESL은 licarbazepine의 거울상이성질체 중 S-licarbazepine이며, S-licarbazepine과 R-licarbazepine의 비율은 약 20:1이다. ESL은 특징적으로 느린 소디움 통로 비활성화(slow Na+ channel inactivation)을 주된 기전으로 하며, 소디움 통로에 대한 선택성과 친화성에서 carbamazepine이나 oxcarbazepine에 비해 우월하다. ESL은 구강 투여 후 간에서 대사되어 소변으로 배출된다. ESL을 병용투여할 경우 carbamazepine, phenytoin, phenobarbital, warfarin, statin, 그리고 경구피임약의 효과가 감소할 수 있으므로 주의가 필요하다.
Carbamazepine과 oxcarbazepine의 한계를 극복한 ESL의 국내 도입으로, 뇌전증 치료에서 새로운 선택지를 확보하게 되었다. 앞으로 ESL의 활약으로 더 나은 뇌전증 치료 성적을 거둘 수 있기를 기대한다.
Notes
Conflicts of interest
No potential conflicts of interest relevant to this article was reported.
Funding
None.
Author contributions
All work was done by KTK and YWC.