|
 |
- Search
| Epilia: Epilepsy Commu > Volume 3(2); 2021 > Article |
|
Abstract
Vagus nerve stimulation (VNS) was approved as an adjunctive therapy for patients with intractable epilepsy in 1999 and has been covered by National Health Insurance in Korea since 2005. VNS is a particularly good option for patients with intractable epilepsy who are not eligible for epilepsy surgery or patients with a high drug load or nonadherence to anticonvulsants. The effect of seizure reduction by VNS tends to gradually increase in proportion to the duration of treatment. Common side effects are usually mild and transient, including voice change, paresthesia in the neck or throat, and cough. The role of VNS is expected to expand in the future as a substantial proportion of patients show better quality of life with improvements in cognition, language, and behavior, as well as seizure reduction.
뇌전증은 연간 10만 명당 50–70명의 발생률을 보이는 주요 뇌질환으로 항경련제가 일차적인 치료이다. 뇌전증 환자의 30%는 2개 이상의 적절한 항경련제에 조절되지 않는 난치성 뇌전증으로 진행하여 항경련제의 추가적인 치료만으로 만족스러운 효과를 기대하기 힘들고, 약물이 늘어남에 따라 부작용도 증가하므로 수술, 식이요법, 신경 전기자극술과 같은 비약물적인 치료를 고려해야 한다.
1930년대에 개, 쥐, 고양이, 원숭이 등 다양한 동물에서 미주신경을 전기로 자극하면 뇌전증 발작이 억제된다는 것을 발견한 후, 1987년 설립된 미국 Cyberonics사(Huston, TX, USA)에서 미주신경 자극 치료장치(VNS TherapyⓇ System)를 생산하기 시작하여, 1988년 Penry와 Dean1이 처음으로 뇌전증 환자에게 삽입하여 발작이 조절되었다고 보고하였다. 이후 1994년 유럽, 1997년 미국, 1999년 우리나라에서 뇌전증의 부가치료법으로 정식 승인을 받게 되었고, 2005년 난치성 국소 뇌전증과 레녹스-가스토 증후군 환자의 치료에 국내 국민건강보험이 적용되면서 우리나라에서도 난치성 뇌전증 환자의 치료로 자리 잡게 되었다.
본 고에서는 뇌전증 환자에서 미주신경 자극술의 전반적인 사항에 대한 최신 지견을 살펴보고, 미주신경 자극술의 이해와 진료에 도움을 주고자 한다.
미주신경 자극술은 체내에 삽입된 장치를 통해 미주신경에 전기적인 자극을 가하여 뇌기능을 변화시킴으로써 치료 효과를 기대하는 방법이다.
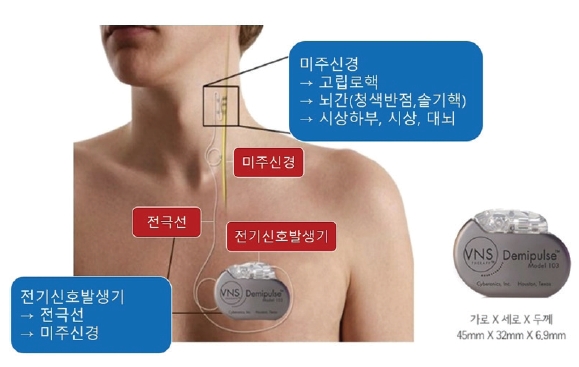
미주신경 자극기는 배터리가 내장된 전기신호 발생기, 전선, 프로그램 막대, 소프트웨어가 설치된 개인용 디지털 단말기나 컴퓨터와 같은 조절장치, 휴대용 자석으로 구성되어 있다. 장치를 삽입하는 시술은 겨드랑이의 피부를 절개하고 전기신호 발생기를 피하로 삽입하여 좌측 쇄골 아래 가슴 부위에 거치시킨 후 전기신호 발생기와 목 부위의 미주신경을 전선으로 연결하는 것이다(Fig. 1).
시술 2주 후 외부 조절장치를 통해 전신신호 발생기를 가동하면 전기신호 발생기에서 전기신호가 전선을 통해서 미주신경으로 전달된다. 프로그램 막대를 전기신호 발생기가 삽입된 부위의 피부에 접촉하면 소프트웨어가 설치된 조절장치에서 현재의 설정을 확인하거나 새로운 설정으로 변경하여 치료의 단계를 조절해 나갈 수 있다. 처음 미주신경 자극을 시작할 때 출력전류 0.25 mA, 자석전류 0.5 mA, 가동시간(signal ON time) 30초, 휴식시간(signal OFF time) 5분, 주파수 30 Hz, 펄스 폭 500 μs로 설정한다. 이후 환자의 발작과 부작용의 반응을 관찰하면서 출력전류를 0.25 mA씩 증가해 간다. 휴대용 자석은 평소 환자 주변에 두거나 휴대하여 전조나 발작이 나타날 때 전기신호 발생기 부위의 피부 위를 스치듯 움직이면 자석에 의해 형성된 전기신호가 전기신호 발생기를 1분간 연속적인 전기자극 모드로 변경하여 발작을 조기 중단시키는 효과를 일부 환자에서 볼 수 있다.
미주신경 자극술이 뇌전증의 치료로 처음 승인되었을 당시 발작 억제 효과가 있다는 것은 알고 있었지만 기전에 대해서는 잘 알려지지 않았다. 이후 많은 동물 및 인체 연구를 통해 점차 기전과 관련된 사실이 밝혀지고 있다.
미주신경은 자율신경계의 부교감신경 기능 조절에 관여하는 뇌신경으로 80%의 감각신경과 20%의 운동신경으로 이루어져 있다. 미주신경에 전기자극을 하면 감각을 뇌로 전달하는 구심신경을 거쳐 고립로핵(nucleus tractus solitarius)으로 신호를 전달한다. 이 자극은 이후 직‧간접적으로 노르에피네프린을 분비하는 청색반점(locus ceruleus)과 세로토닌을 분비하는 솔기핵(raphe nuclei)을 통해 소뇌, 시상, 시상하부, 편도, 해마, 뇌섬, 대뇌피질로 여러 단계의 시냅스 경로를 거쳐 신호를 전달하여, 결과적으로 광범위한 뇌 부위의 혈류와 전기적인 흥분성에 영향을 주게 된다(Fig. 2).
미주신경 자극을 뇌로 전달되는 경로에서 특히 중요한 중개핵은 청색반점과 솔기핵으로서, 이 부위를 손상시키면 미주신경에 전기자극을 주어도 발작 억제 효과가 나타나지 않는다. 청색반점과 솔기핵이 각각 분비하는 신경전달물질인 노르에피네프린과 세로토닌의 농도를 증가시키는 약물은 발작을 억제하는 효과가 있고, 반대로 노르에피네프린과 세로토닌 농도를 감소시키는 약물은 발작을 증가시키는 효과가 있다는 사실을 여러 연구에서 보고하고 있다. 또한 미주신경 자극술 치료를 하게 되면 뇌척수액에서 발작을 억제하는 gamma-aminobutyric acid가 증가하고 발작을 증가시키는 aspartate가 감소하는 현상도 관찰된다. 이러한 증거를 볼 때 미주신경 자극술의 발작 억제 효과는 미주신경의 전기자극에 의해 분비되는 노르에피네프린과 세로토닌을 중개로 발생하는 전반적 뇌 활동의 전기적, 화학적 변화에 의해 나타난다고 생각된다.
미주신경 자극술의 대상이 되는 뇌전증 환자의 조건으로는 (1) 최소 2가지 이상의 적절한 항경련제에 조절되지 않는 약물난치성 뇌전증, (2) 내측두엽 뇌전증이나 절제 가능한 병변이 있는 국소 뇌전증과 같이 뇌전증 수술의 적절한 대상이 되지 않는 뇌전증, (3) 발작이 비뇌전증 발작이 아닌 것이 확인된 경우를 들 수 있다. 연령, 성별, 발작 유형, 뇌전증 증후군, 원인, 발작의 빈도, 사용한 항경련제로 미주신경 자극술의 효과를 예측하기는 힘들다. 뇌전증 환자 중 뇌량 절제술을 고려하는 환자나 재수술이 필요한 뇌전증 환자에서도 미주신경 자극술이 유용하고 뇌수술에 비해 더 안전하다는 보고가 있다.2,3 많은 항경련제 복용으로 인지와 정서 등 뇌기능의 저하가 있는 환자, 약물 순응도가 낮은 환자, 발달이 중요한 어린 연령의 환자는 미주신경 자극술이 이러한 문제나 부작용을 줄일 수 있어서 좋은 대상이 될 수 있다.
1997년 미국에서 처음 난치성 뇌전증 환자의 치료로 승인을 받은 후 유럽과 아시아 등 세계 수십 개 국가에서 뇌전증의 치료로 사용하고 있으나 의료보험의 적용 기준은 국가에 따라 다르다. 우리나라는 2005년부터 항경련제 치료에도 2년 이상 조절되지 않는 난치성 국소 뇌전증과 레녹스-가스토 증후군 환자의 부가요법으로 국민건강보험을 적용하고 있다. 그러나 특정 발작 유형이나 뇌전증 증후군과 관련 없이 모든 난치성 뇌전증에서 발작 감소와 삶의 질의 개선을 보인다는 자료가 지속적으로 보고되고 있으므로 현재 많은 국가에서 미주신경 자극술의 대상을 모든 난치성 뇌전증 환자로 확대하여 실시하고 있다. 우리나라도 미주신경 치료의 도움을 받을 수 있는 모든 난치성 뇌전증 환자가 혜택을 받을 수 있도록 제도의 개선이 필요하다고 하겠다.
미주신경 자극술의 절대적인 금기 대상은 과거에 좌측 또는 양측 경부 미주신경의 절제술을 받은 환자이다. 심장질환이나 폐질환이 있는 환자는 절대적인 금기 대상은 아니지만 미주신경 자극술이 기존 증상에 영향을 줄 수도 있으므로 시술 전후 심폐기능의 평가가 필요하다. 폐쇄성 수면 무호흡증 환자는 미주신경 자극술로 인해 무호흡이 증가할 수 있으나 임상적으로 문제가 있는 경우는 흔하지 않으며, 자극 강도를 낮추면 예방이 가능하고, 오히려 미주신경 자극에 의해 깊은 수면이 증가하는 효과로 발작이 감소하는 이점도 있으므로 절대적인 금기 대상에 해당하지 않는다.4-6
미주신경 자극술이 발작 감소에 효과가 있다는 것은 많은 연구를 통해 잘 알려져 있다. 발작 감소와 함께 또는 별개로 인지와 행동이 호전되고 전반적인 삶의 질이 호전된다는 연구도 다양하게 발표되고 있다. 발작 감소 효과는 수개월의 단기간뿐만 아니라 수년 이상 장기적으로도 효과가 유지되거나 증가하는 양상을 보인다.
중요한 임상연구로 114명의 국소발작 환자를 대상으로 한 무작위 대조연구인 EO3 연구에서 치료 효과 이하의 낮은 강도와 치료 효과를 보이는 높은 강도 자극의 두 군으로 나누어 시술 12주 후 비교한 결과, 50% 이상 발작 감소를 보인 환자에서 높은 강도 자극을 준 군이 두 배로 높게 나와서 미주신경 자극술이 단기간의 발작 감소에 효과가 있음을 확인하였다(31% vs. 14%).7
EO5 연구는 더 많은 199명의 국소발작 환자를 대상으로 한 무작위 대조연구인데, 3개월 후 50% 이상 발작 감소를 보이는 환자가 23.4%임을 확인하였고 전조 여부에 따른 차이는 없었다.8 대조 연구를 종료한 이후 장기 추적을 하여 발작 빈도 감소율이 3개월 후 20%, 2년 후 45%임을 확인하여, 단기간뿐만 아니라 장기적으로 발작 감소가 유지된다는 점과 치료 기간이 길어질수록 치료 효과가 증가한다는 것을 보여주었다.9
미주신경 자극기 시판 후 소아와 성인을 6개월 간격으로 10년 이상의 추적한 장기 연구에서는 50% 이상 발작 감소 효과를 보인 환자의 비율이 추적 기간에 비례해서 증가하여 마지막 방문 시점을 기준으로 91%에 도달하였다. 치료 기간에 따른 발작 감소 환자의 증가 추세는 첫 2년간 빠른 속도로 증가하였으나 이후에도 장기적으로 증가하는 경향을 보여주었으며, 이는 미주신경 자극술과 항경련제 조절의 동반 상승효과로 생각된다.10 12개월 이상 평균 44개월 추적한 다기관 연구에서는 50% 이상 발작 감소 환자가 59%, 완전 발작 조절이 된 환자도 9%에서 관찰되었다.11 소아에 국한한 난치성 뇌전증 환자의 메타분석 연구에서도 최종 추적 시(평균 2.5년)에 50% 이상 발작 감소 환자와 완전 조절 환자가 각각 56.4%, 11.6%로 비슷한 결과를 보여주었다.12
미주신경 자극술을 시작한 후 1년 이상 도중에 항경련제를 변경하지 않고 추적한 연구가 있었는데, 50% 이상 발작 감소된 환자가 3개월 후 45%, 12개월 후 58%에 달하여 미주신경 자극술의 치료효과는 항경련제의 효과와는 독립적으로 나타나며 역시 시간에 따라 증가함을 보여주었다.13 다른 전향적 연구에서는 발작 빈도 뿐만 아니라 발작 지속시간과 발작 후 억제 시간도 감소한다고 보고하였다.14,15
미주신경 자극의 효과에 관한 동물연구에서는 이미 시작된 급성 발작을 빨리 끝내는 효과와 자극을 주어도 급성 발작이 일어나지 않도록 하는 예방효과뿐 아니라 뇌전증 동물에서 발작을 감소시키고, 특정 뇌 부위의 반복 자극으로 뇌전증을 일으키는 동물 킨들링(kindling) 모델에서 뇌전증 생성(epileptogenesis)을 억제하여 뇌전증으로 진행하는 것을 예방하는 효과를 보여주었다.16
미주신경 자극술에 좋은 반응을 보이는 특정한 환자군에 대한 여러 연구에서는 치료 시작 시의 환자 연령, 발작 형태, 특정한 뇌전증 증후군에 따른 치료 효과의 차이는 없다고 보고하고 있다. 그러나 18세 이하 소아 및 청소년을 대상으로 한 연구에서는 특히 12세 이하 소아에서 효과가 더 좋았으며,17 그 중 레녹스-가스토 증후군, 시상하부 과오종, 뇌전증 뇌증, 레트 증후군, 드라베 증후군, 결정성 경화증에서 효과가 좋았다는 보고들이 있다. 또한 발작 감소뿐 아니라 언어 수행능력, 각성 수준, 운동기능, 인지기능, 전반적 행동, 삶의 질에 호전을 보이는 환자들이 많았으며, 일부에서는 극적인 개선을 보이기도 하였다. 이와 비슷한 효과는 노인의 연령에서도 관찰되었다.
수술과 관련된 합병증은 드물다. 초기 모델에서 전선이 절단되는 합병증이 있었으나 개선된 모델에서는 거의 발생하지 않는다. 감염이 1%에서 발생할 수 있으나 항생제 치료로 대부분 호전되므로 장치 제거가 필요한 경우는 별로 없으며, 성대 마비가 1%에서 발생할 수 있으나 보통 몇 주에 걸쳐 회복된다.18
전기자극을 시작하면서 자극의 강도와 관련된 부작용이 관찰될 수 있으나 대부분 가벼운 증상으로 나타난다(Table 1).19 이러한 증상으로 목소리 변화, 목에 통증이나 이상 감각, 목이 조이는 느낌이나 숨쉬기가 답답한 증상, 기침 등이 있으나 자극의 강도를 줄이면 호전되며, 시간이 지나면서 점차 사라지므로 이로 인해 치료를 중단하는 경우는 별로 없다.20 일부에서 침 분비가 증가하거나 음식 삼키는 것이 힘든 연하곤란이 나타나는 경우가 있는데 이때는 식사할 때 자석을 전기신호 발생기 위에 부착하여 일시적으로 미주신경 자극을 중단하는 방법을 사용할 수 있다.21 미주신경 자극의 주파수를 50 Hz 미만으로 하고 자극시간을 휴식시간보다 짧게 설정하면 장기간 전기자극을 주더라도 미주신경의 손상이 발생하지 않는다.22 주요 정신질환 과거력이 있는 환자에서, 특히 매일 발작을 하는 경우 정신과적 증상이 나타나는 경우가 있다는 보고가 있는데 이때는 정신과 약물치료를 병행하거나 미주신경 자극의 강도를 줄이면 호전될 수 있다.23
전신 증상은 거의 발생하지 않는다. 폐질환이 없는 환자에서 미주신경 자극술 전후 폐기능검사에 의미 있는 변화는 없으나, 이전에 심한 폐질환이 있던 환자에서 강한 자극 시 폐기능이 감소되는 경우가 있으므로 이때는 기관지 확장제를 투여하거나 자극 강도나 주파수를 낮추도록 한다. 미주신경 자극술은 임상적으로 의미 있는 심장기능, 소화기능, 혈액검사 이상을 초래하지 않으며, 복용하는 약물 농도, 활력징후, 체중에도 영향을 미치지 않는다.
미주신경 자극술은 항경련제 치료에 비해 여러 장점이 있다. 발작 조절에 효과가 있으면서 전체 항경련제의 부담을 증가시키지 않으므로 신경계와 전신에 약물로 인한 부작용이 없으며, 기존에 복용하고 있는 여러 항경련제와 약물 상호작용을 우려할 필요가 없다. 발작의 감소 효과뿐 아니라 각성 수준, 집중력, 기억력, 감정, 의사소통 능력 등 인지기능이 호전되어 환자의 삶의 질이 나아지고, 깨어있는 낮 시간에 좀 더 명료하게 되는 효과가 있다.24-32 또한 약물 복용이나 식이요법과는 달리 환자의 적극적인 참여가 없이도 치료 효과가 유지되므로 치료의 순응도가 떨어지는 환자에게 특히 도움이 된다.33,34 발작이 발생하면 자석으로 발작을 빨리 중단할 수 있는 효과를 보이는 환자에서는 뇌전증을 통제할 수 있다는 자신감을 줄 수 있다. 동물실험에서 불임이나 태아에 기형을 일으키지 않았으며, 사람에서도 임산부에서 건강한 아기를 출산하였다고 보고하고 있다.35-37
단점으로는 시술비용의 문제를 들 수 있는데 장기적으로 시간이 지남에 따라 오히려 의료비용을 상쇄하여 1년 반 이후부터는 실제 의료비용이 감소한다는 연구보고가 있다.33 이는 약제비와 응급실 방문, 입원 횟수와 입원 일수, 대발작으로 인한 골절이나 두부 외상과 같은 부상이 감소하고, 이로 인해 외래 방문일수와 결석 및 결근 일수도 감소하는 것과 관계가 있다.33,38 미주신경 자극기 삽입 후 자기공명영상 검사가 필요한 경우에는 3 Tesla 이하로 촬영하고 필요 시 특수 수신 코일을 이용하며, 검사 전에 전기신호 발생기의 전류를 끄고 검사가 끝난 후 다시 본래대로 작동을 해야 하는 등의 주의가 필요하다.
Acknowledgements
This study was supported by a 2021 research grant from Pusan National University Yangsan Hospital.
Fig. 2.
Mechanism of electric and chemical signal transmission to the brain by vagus nerve stimulation. Electrical stimuli on the vagus nerve are transmitted to nucleus tractus solitarius, in turn triggering locus ceruleus and raphe nuclei in the brain stem. Norepinephrine and serotonin secreted from the locus ceruleus and raphe nuclei affect widespread areas in the brain, including the thalamus, hypothalamus, amygdala, insula, hippocampus, striatum, and cerebral cortex.

Table 1.
Common side effects of vagus nerve stimulation
| Side effect | Frequency (%) |
|---|---|
| Voice change | 38 |
| Increased cough | 5 |
| Dysphonia | <5 |
| Cervical pain or paresthesia | <5 |
| Exertional dyspnea | <5 |
| Hypersialorrhea or dysphagia | <5 |
| Dyspepsia | <5 |
Adapted from Toffa et al. 19
References
1. Penry JK, Dean JC. Prevention of intractable partial seizures by intermittent vagal stimulation in humans: preliminary results. Epilepsia 1990;31 Suppl 2:S40–S43.


2. Lancman G, Virk M, Shao H, et al. Vagus nerve stimulation vs. corpus callosotomy in the treatment of Lennox-Gastaut syndrome: a meta-analysis. Seizure 2013;22:3–8.


3. Elliott RE, Morsi A, Geller EB, Carlson CC, Devinsky O, Doyle WK. Impact of failed intracranial epilepsy surgery on the effectiveness of subsequent vagus nerve stimulation. Neurosurgery 2011;69:1210–1217.


4. Malow BA, Edwards J, Marzec M, Sagher O, Fromes G. Effects of vagus nerve stimulation on respiration during sleep: a pilot study. Neurology 2000;55:1450–1454.


5. Hsieh T, Chen M, McAfee A, Kifle Y. Sleep-related breathing disorder in children with vagal nerve stimulators. Pediatr Neurol 2008;38:99–103.


6. Hallböök T, Lundgren J, Köhler S, Blennow G, Strömblad LG, Rosén I. Beneficial effects on sleep of vagus nerve stimulation in children with therapy resistant epilepsy. Eur J Paediatr Neurol 2005;9:399–407.


7. Handforth A, DeGiorgio CM, Schachter SC, et al. Vagus nerve stimulation therapy for partial-onset seizures: a randomized active-control trial. Neurology 1998;51:48–55.


8. The Vagus Nerve Stimulation Study Group. A randomized controlled trial of chronic vagus nerve stimulation for treatment of medically intractable seizures. Neurology 1995;45:224–230.


9. Salinsky MC, Uthman BM, Ristanovic RK, Wernicke JF, Tarver WB. Vagus nerve stimulation for the treatment of medically intractable seizures. Results of a 1-year open-extension trial. Vagus Nerve Stimulation Study Group. Arch Neurol 1996;53:1176–1180.


10. Elliott RE, Morsi A, Tanweer O, et al. Efficacy of vagus nerve stimulation over time: review of 65 consecutive patients with treatment-resistant epilepsy treated with VNS > 10 years. Epilepsy Behav 2011;20:478–483.


11. De Herdt V, Boon P, Ceulemans B, et al. Vagus nerve stimulation for refractory epilepsy: a Belgian multicenter study. Eur J Paediatr Neurol 2007;11:261–269.


12. Jain P, Arya R. Vagus nerve stimulation and seizure outcomes in pediatric refractory epilepsy: systematic review and meta-analysis. Neurology 2021;Apr 13; [Epub].https://doi.org/10.1212/wnl.0000000000012030.

13. Labar D. Vagus nerve stimulation for 1 year in 269 patients on unchanged antiepileptic drugs. Seizure 2004;13:392–398.


14. Ardesch JJ, Buschman HP, Wagener-Schimmel LJ, van der Aa HE, Hageman G. Vagus nerve stimulation for medically refractory epilepsy: a long-term follow-up study. Seizure 2007;16:579–585.


15. Abubakr A, Wambacq I. Long-term outcome of vagus nerve stimulation therapy in patients with refractory epilepsy. J Clin Neurosci 2008;15:127–129.


16. Fernández-Guardiola A, Martínez A, Valdés-Cruz A, Magdaleno-Madrigal VM, Martínez D, Fernández-Mas R. Vagus nerve prolonged stimulation in cats: effects on epileptogenesis (amygdala electrical kindling): behavioral and electrographic changes. Epilepsia 1999;40:822–829.


17. Alexopoulos AV, Kotagal P, Loddenkemper T, Hammel J, Bingaman WE. Long-term results with vagus nerve stimulation in children with pharmacoresistant epilepsy. Seizure 2006;15:491–503.


18. Fernando DA, Lord RS. The blood supply of vagus nerve in the human: its implication in carotid endarterectomy, thyroidectomy and carotid arch aneurectomy. Ann Anat 1994;176:333–337.


19. Toffa DH, Touma L, El Meskine T, Bouthillier A, Nguyen DK. Learnings from 30 years of reported efficacy and safety of vagus nerve stimulation (VNS) for epilepsy treatment: a critical review. Seizure 2020;83:104–123.


20. Liporace J, Hucko D, Morrow R, et al. Vagal nerve stimulation: adjustments to reduce painful side effects. Neurology 2001;57:885–886.


21. Lundgren J, Ekberg O, Olsson R. Aspiration: a potential complication to vagus nerve stimulation. Epilepsia 1998;39:998–1000.


22. Cyberonics, Inc. VNS therapy physician’s manual [Internet]. Houston, TX: Cyberonics, Inc.; 2006 [cited 2021 Sep 17]. Available from: http://www.vnstherapy.com/epilepsy/hcp/manuals/default.aspx.
23. Blumer D, Davies K, Alexander A, Morgan S. Major psychiatric disorders subsequent to treating epilepsy by vagus nerve stimulation. Epilepsy Behav 2001;2:466–472.


24. Hammond EJ, Uthman BM, Reid SA, Wilder BJ. Electrophysiological studies of cervical vagus nerve stimulation in humans: I. EEG effects. Epilepsia 1992;33:1013–1020.


25. Clarke BM, Upton AR, Griffin H, Fitzpatrick D, DeNardis M. Chronic stimulation of the left vagus nerve in epilepsy: balance effects. Can J Neurol Sci 1997;24:230–234.


26. Clarke BM, Upton AR, Griffin H, Fitzpatrick D, DeNardis M. Chronic stimulation of the left vagus nerve: cognitive motor effects. Can J Neurol Sci 1997;24:226–229.


27. Harden CL, Pulver MC, Ravdin LD, Nikolov B, Halper JP, Labar DR. A pilot study of mood in epilepsy patients treated with vagus nerve stimulation. Epilepsy Behav 2000;1:93–99.


28. Clark KB, Naritoku DK, Smith DC, Browning RA, Jensen RA. Enhanced recognition memory following vagus nerve stimulation in human subjects. Nat Neurosci 1999;2:94–98.


29. Ghacibeh GA, Shenker JI, Shenal B, Uthman BM, Heilman KM. The influence of vagus nerve stimulation on memory. Cogn Behav Neurol 2006;19:119–122.


30. Cramer JA. Exploration of changes in health-related quality of life after 3 months of vagus nerve stimulation. Epilepsy Behav 2001;2:460–465.


31. Malow BA, Edwards J, Marzec M, Sagher O, Ross D, Fromes G. Vagus nerve stimulation reduces daytime sleepiness in epilepsy patients. Neurology 2001;57:879–884.


32. Galli R, Bonanni E, Pizzanelli C, et al. Daytime vigilance and quality of life in epileptic patients treated with vagus nerve stimulation. Epilepsy Behav 2003;4:185–191.


33. Helmers SL, Duh MS, Guérin A, et al. Clinical and economic impact of vagus nerve stimulation therapy in patients with drug-resistant epilepsy. Epilepsy Behav 2011;22:370–375.


34. Helmers SL, Duh MS, Guérin A, et al. Clinical outcomes, quality of life, and costs associated with implantation of vagus nerve stimulation therapy in pediatric patients with drug-resistant epilepsy. Eur J Paediatr Neurol 2012;16:449–458.


35. Danielsson I, Lister L. A pilot study of the teratogenicity of vagus nerve stimulation in a rabbit model. Brain Stimul 2009;2:41–49.


36. Ben-Menachem E, Hellström K, Waldton C, Augustinsson LE. Evaluation of refractory epilepsy treated with vagus nerve stimulation for up to 5 years. Neurology 1999;52:1265–1267.


-
METRICS

-
- 0 Crossref
- 3,303 View
- 47 Download
- Related articles in Epilia: Epilepsy Commun
-
Diagnosis and Treatment of Depression in Patients with Epilepsy2022 September;4(2)
Felt Stigma in Korean Persons with Epilepsy2021 September;3(2)
Physical Exercise in Patients with Epilepsy2021 March;3(1)
Contraception for Women with Epilepsy2020 September;2(2)
Prospects of Seizure Prediction Technology for Patients with Epilepsy2020 September;2(2)